Показана перспективность создания нового лекарственного средства с психотропной активностью в результате изучения химического состава и фармакологической активности модифицированных сухих экстрактов пустырника сердечного. Наиболее перспективными веществами оказались сухие экстракты, модифицированные добавлением небольших количеств аргинина, валина, фенилаланина, глицина, лизина и аланина. Всего в экстрактах обнаружено 15 основных фенольных веществ, из них идентифицировано 8. В этих экстрактах также было 10 гидроксикоричных кислот, три из которых были идентифицированы (хлорогеновая, кофейная и розмариновая кислоты). Доминирующими гидроксикоричными кислотами были хлорогеновая и кофейная кислоты. Среди флавоноидов идентифицированы катехин, гиперозид и рутин. Следует отметить, что экстракты имели значительное содержание эллаговой кислоты. На основании результатов фитохимического анализа экстрактов можно сделать вывод, что состав фенольных соединений существенно не отличается, а основные отличия связаны с аминокислотами, которые, очевидно, оказывают влияние на общий фармакологический эффект. Полученные результаты свидетельствуют о наличии анксиолитической активности у исследуемых экстрактов пустырника в комплексе с аминокислотами. Экстракты с глицином, валином и аргинином оказались более эффективными в снижении тревожности у животных.
1. Введение
В условиях современного ритма жизни чаще возникают нарушения со стороны центральной нервной системы (ЦНС), связанные с чрезмерной возбудимостью и повышенной тревожностью. Хронический стресс и эмоциональные перегрузки приводят к появлению симптомов неврогенных и психосоматических заболеваний. По данным Всемирной организации здравоохранения (ВОЗ) (2017 г.), депрессия занимает первое место в мире среди других заболеваний, поражая около 300 млн человек, а биполярное расстройство занимает второе место. По результатам современных исследований 60–90 % обращений к врачам связаны со стрессовыми состояниями. Для медикаментозной коррекции таких нарушений в основном используют седативные средства и анксиолитики. При выборе седативных препаратов более 80% населения отдают предпочтение продуктам растительного происхождения.
Трава пустырника сердечного ( пустырник сердечный) является одним из наиболее широко используемых седативных лекарственных растений. В литературе представлены значительные научные данные по изучению химического состава представителей рода пустырника . В целом из этого рода выделено и определено строение около 270 веществ. Они представлены алкалоидами монотерпеноидами, сесквитерпеноидами, дитерпеноидами, тритерпеноидами, иридоидами, флавоноидами, фенилпропаноидами, стероидами и циклические пептиды. Большинство научных первоисточников сосредоточено на изучении алкалоидов (леонурин и стахидрин) и дитерпеноидов (147 дитерпеноидов лабданума). В большей степени изучены надземные части представителей рода Leonurus.
Препараты пустырника впервые были использованы в медицинской практике как кардиотонические средства, регулирующие ритм сердечной деятельности, при стенокардии, сердечно-сосудистых неврозах, начальных стадиях гипертонической болезни. Лишь в начале 20 века его стали использовать как успокаивающее средство, усиливающее процессы торможения или уменьшающее процессы возбуждения в ЦНС. В настоящее время его применяют при кардиосклерозе, повышении артериального давления, стенокардии, миокардите, кардионеврозе, повышенной нервной возбудимости, особенно при ее сочетании с климактерией у женщин и гипертрофией предстательной железы у мужчин, неврастении, сопровождающейся бессонницей, чувством напряжения и повышенной реактивности, а также вегетативных неврозов. Препараты пустырника показаны при эпилепсии, гипоменструальном синдроме, базедовой болезни, заболеваниях желудочно-кишечного тракта и др. Модификация фитопрепаратов приводит к повышению их активности и появлению новых фармакологических эффектов биологически активных веществ (БАВ), например, анксиолитической и диуретической активности.
Травяные средства или сухое сырье составляют многие лекарства. Одним из наиболее распространенных лекарственных средств на основе этого лекарственного растения является настойка пустырника. Способ получения настойки пустырника хорошо известен. Однако недостатком этого препарата является нестабильность химического состава и, как следствие, фармакодинамики. Кроме того, при изготовлении настоек в качестве экстрагента используется этиловый спирт, что не только ограничивает круг больных, которым можно применять данный препарат (дети, беременные женщины, кормящие матери, лица, деятельность которых требует повышенного внимания и т. д.), но, в свою очередь, также способен воздействовать на ЦНС и модулировать действие самого препарата. Поэтому этим категориям больных рекомендуется прием водных экстрактов этого сырья, но эти лекарственные формы не стандартизированы, плохо хранятся, имеют различный химический состав. В связи с этим разработка стандартизированных лекарственных средств на основе настойки травы пустырника, не содержащих в своем составе этанола, является актуальной задачей.
Ранее была обоснована технология получения сухой настойки травы пустырника. Он предполагает замену спирта сухим вспомогательным веществом (сахароза, маннит, сорбит и др.). Полученный продукт имеет благоприятные технологические показатели: удовлетворительные объемные свойства, меньшую гигроскопичность, стабильность при хранении.
Аминокислоты в экстрактах способны образовывать соли, комплексы и конъюганты с другими группами БАВ, например, с фенольными соединениями, что изменяет их физико-химические свойства, влияет на растворимость, биодоступность и общий фармакологический эффект, приводит к увеличению их активность и появление новых фармакологических эффектов. Поэтому модификация настойки пустырника с использованием аминокислот и добавлением вспомогательных веществ для создания новых сухих экстрактов является актуальной задачей современной фармации.
Цель работы - изучение фитохимического профиля и психотропной активности модифицированных сухих экстрактов настойки пустырника.
2. Результаты
2.1. Фитохимические исследования
Настойка пустырника, использованная для получения модифицированных экстрактов, полностью соответствовала требованиям ГФУ 2.0 «Настойка пустырника Н». Сухой остаток в настойке составил 2,04 ± 0,03 %, при этом содержание фенольных соединений в сухом остатке настойки составило 8,17 ± 0,06 %.
Полученные модифицированные сухие экстракты представляли собой порошки зеленовато-коричневого цвета с характерным запахом. В результате тонкослойной хроматографии (ТСХ) анализа полученных сухих экстрактов выделены следующие группы биологически активных веществ (БАВ): флавоноиды (рутин и гиперозид), производные гидроксикоричных кислот (хлорогеновая, кофейная и розмариновая кислоты) и иридоидные соединения (гарпагид, гарпагид ацетат и аюгозид).
Полученные экстракты анализировали методом ВЭЖХ (Таблица 1). В результате исследования экстракты пустырника показали достаточно близкий химический состав фенольных соединений, так как в качестве исходного сырья использовалась одна и та же настойка. С другой стороны, во многих случаях различие между содержанием БАВ в экстрактах с аминокислотами и без них считалось чрезвычайно статистически значимым ( p< 0,0001). В экстрактах обнаружено 15 основных веществ фенольной природы, из них идентифицировано 8. В этих экстрактах также было 10 гидроксикоричных кислот, три из которых были идентифицированы (хлорогеновая, кофейная и розмариновая кислоты). Доминирующими гидроксикоричными кислотами были хлорогеновая и кофейная кислоты. Среди флавоноидов идентифицированы катехин, гиперозид и рутин. Следует отметить, что экстракты имели значительное содержание эллаговой кислоты.
Таблица 1. Результаты анализа модифицированных экстрактов пустырника методом ВЭЖХ.
| Компонент |
Количественное содержание в экстракте, мг/100 г, |
||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Экстракт с настойкой пустырника | С лизином | С аспарагиновой кислотой | С лейцином | С Аланиной | С фенилаланином | С глицином | С валином | С гистидином | С глутаминовой кислотой | С аргинином | С цистеином | С метионином | |
|
Производные кофейной кислоты-1 |
1,79 ± 0,04 # | 2,37 ± 0,08 | 1,86 ± 0,03 | 1,72 ± 0,04 | 1,89 ± 0,03 | 2,17 ± 0,05 | 1,93 ± 0,02 | 2,47 ± 0,05 | 2,52 ± 0,04 | 1,67 ± 0,03 | 1,84 ± 0,02 | 1,73 ± 0,03 | 1,61 ± 0,02 |
|
Производные кофейной кислоты-2 |
2,36 ± 0,07 * | 2,17 ± 0,04 | 2,63 ± 0,06 | 1,94 ± 0,02 | 2,52 ± 0,04 | 2,85 ± 0,04 | 2,35 ± 0,06 | 2,18 ± 0,07 | 2,69 ± 0,03 | 2,02 ± 0,02 | 2,47 ± 0,05 | 2,38 ± 0,05 | 2,13 ± 0,08 |
| Хлорогеновая кислота | 76,87 ± 0,57 # | 65,88 ± 0,87 | 71,3,8 ± 0,87 | 78,79 ± 0,93 | 76,38 ± 0,76 | 69,74 ± 0,77 | 75,69 ± 0,91 | 79,84 ± 0,84 | 75,27 ± 0,99 | 80,16 ± 0,74 | 76,19 ± 0,95 | 75,97 ± 0,69 | 74,84 ± 0,97 |
| Кофеиновая кислота | 5,58 ± 0,11 * | 5,08 ± 0,17 | 6,15 ± 0,18 | 6,24 ± 0,27 | 5,69 ± 0,13 | 5,18 ± 0,15 | 5,82 ± 0,14 | 5,93 ± 0,09 | 5,57 ± 0,09 | 4,98 ± 0,06 | 5,29 ± 0,16 | 5,14 ± 0,17 | 5,37 ± 0,41 |
|
Производные кофейной кислоты-3 |
3,68 ± 0,08 # | 3,39 ± 0,05 | 3,78 ± 0,11 | 3,66 ± 0,09 | 3,32 ± 0,08 | 3,79 ± 0,11 | 3,08 ± 0,06 | 3,26 ± 0,12 | 3,68 ± 0,05 | 3,58 ± 0,06 | 2,97 ± 0,07 | 3,16 ± 0,14 | 3,05 ± 0,21 |
|
Производные кофейной кислоты-4 |
14,4 ± 0,2 # | 11,8 ± 0,1 | 13,7 ± 0,2 | 12,9 ± 0,2 | 8,9 ± 0,1 | 13,2 ± 0,2 | 15,8 ± 0,2 | 11,9 ± 0,2 | 16,4 ± 0,4 | 11,6 ± 0,2 | 13,2 ± 0,4 | 15,7 ± 0,4 | 7,5 ± 0,2 |
|
Derivatives of caffeic acid-5 |
1.27 ± 0.02 # | 0.98 ± 0.01 | 1.04 ± 0.01 | 0.87 ± 0.01 | nd | 1.21 ± 0.02 | 0.95 ± 0.01 | 0.93 ± 0.01 | 1.13 ± 0.03 | 1.23 ± 0.03 | 1.17 ± 0.02 | nd | 0.87 ± 0.01 |
| Rutin | 1.20 ± 0.01 # | 1.07 ± 0.02 | 1.16 ± 0.01 | 1.27 ± 0.01 | 1.31 ± 0.02 | 0.98 ± 0.01 | 1.17 ± 0.01 | 1.26 ± 0.01 | 1.17 ± 0.01 | 1.24 ± 0.01 | 1.18 ± 0.02 | 0.95 ± 0.01 | 1.01 ± 0.01 |
| Ellagic acid | 41.65 ± 0.97 ** | 40.87 ± 0.67 | 37.93 ± 0.73 | 40.10 ± 0.57 | 37.69 ± 0.83 | 42.38 ± 0.55 | 41.31 ± 0.63 | 40.87 ± 0.67 | 42.16 ± 0.29 | 39.17 ± 0.62 | 40.38 ± 0.37 | 40.29 ± 0.91 | 39.79 ± 0.72 |
| Hyperoside | 2.10 ± 0.06 * | 2.28 ± 0.10 | 1.87 ± 0.04 | 2.04 ± 0.06 | 2.18 ± 0.04 | 1.98 ± 0.03 | 2.09 ± 0.04 | 2.18 ± 0.05 | 2.39 ± 0.06 | 2.18 ± 0.03 | 2.08 ± 0.06 | 2.12 ± 0.03 | 2.07 ± 0.03 |
| Rosmarinic acid | 1.72 ± 0.03 *** | 1.54 ± 0.04 | 1.68 ± 0.07 | 2.01 ± 0.03 | 2.21 ± 0.05 | 1.81 ± 0.04 | 1.75 ± 0.02 | 1.61 ± 0.04 | 1.58 ± 0.02 | 1.52 ± 0.03 | 1.48 ± 0.02 | 1.63 ± 0.02 | 1.54 ± 0.01 |
|
Derivatives of caffeic acid-6 |
0.97 ± 0.01 # | 0.86 ± 0.01 | nd | 0.59 ± 0.03 | 0.43 ± 0.01 | nd | 0.76 ± 0.01 | 0.86 ± 0.01 | 0.70 ± 0.01 | 0.92 ± 0.01 | nd | 0.58 ± 0.02 | 0.43 ± 0.01 |
|
Derivatives of caffeic acid-7 |
0.47 ± 0.01 # | 0.41 ± 0.01 | nd | nd | 0.39 ± 0.01 | nd | 0.35 ± 0.01 | nd | 0.37 ± 0.01 | 0.48 ± 0.01 | nd | nd | 0.51 ± 0.01 |
| Catechin | 6.25 ± 0.17 ** | 5.73 ± 0.12 | 6.38 ± 0.07 | 6.02 ± 0.07 | 5.87 ± 0.07 | 5.92 ± 0.11 | 6.01 ± 0.09 | 6.24 ± 0.17 | 6.52 ± 0.16 | 6.08 ± 0.12 | 5.92 ± 0.31 | 5.86 ± 0.63 | 6.17 ± 0.27 |
| Methoxy apigenin | 3.95 ± 0.07 # | 3.48 ± 0.09 | 3.35 ± 0.07 | 4.01 ± 0.07 | 3.75 ± 0.12 | 4.06 ± 0.17 | 3.86 ± 0.13 | 3.39 ± 0.09 | 3.52 ± 0.08 | 3.68 ± 0.07 | 4.12 ± 0.24 | 3.86 ± 0.41 | 3.73 ± 0.21 |
| The amount of flavonoids | 13.50 | 12.56 | 12.76 | 13.34 | 13.11 | 12.94 | 13.13 | 13.07 | 13.60 | 13.18 | 13.30 | 12.79 | 1298 |
| The amount of hydroxycinnamic acids | 109.11 | 94.48 | 102.22 | 108.72 | 101.73 | 99.95 | 108.48 | 108.98 | 109.91 | 108.16 | 104.61 | 106.29 | 97.85 |
| The amount of identified substances | 164.26 | 147.91 | 152.91 | 162,16 | 152,53 | 155,27 | 162,92 | 162,92 | 165,67 | 160,51 | 158,29 | 159,37 | 150,62 |
Различия в содержании биологически активных веществ (БАВ) в экстрактах с аминокислотами и без них по t -критерию считались # чрезвычайно статистически значимыми ( p < 0,0001), * не статистически значимыми ( p = 0,34–0,97). , ** очень статистически значимо ( p = 0,0004–0,015) или *** не вполне статистически значимо ( p = 0,08); нд – не обнаружено.
Хроматограммы модифицированных экстрактов были довольно схожими. Если образовывались устойчивые ковалентные связи, то на хроматограммах они проявлялись как новые вещества. По нашей гипотезе, это позволяет предположить, что аминокислоты образовывали конъюгаты, соли или комплексы с фенольными соединениями и иридоидами, которые легко разрушались кислотой хроматографической системы.
Кроме того, в экстрактах определяли количественное содержание флавоноидов, иридоидов и полифенолов спектрофотометрическим методом (Таблица 2 и Таблица 3). Полученные результаты фитохимического анализа использовали для стандартизации полученных экстрактов, для которых проводили изучение психотропной активности. Содержание основных групп БАВ в полученных экстрактах статистически значимо не различалось ( р = 0,27–0,64), так как сырье – настойка пустырника – одно и то же и взято в одинаковых количествах. Их сравнивали с литературными данными фитохимических исследований настойки пустырника другими авторами. По результатам фитохимического анализа экстрактов можно сделать вывод, что состав фенольных соединений существенно не отличался, а основные отличия относились к аминокислотам, что, очевидно, сказалось на общем фармакологическом эффекте.
Таблица 2. Количественное содержание основных групп БАВ в модифицированных экстрактах пустырника.
| Извлекать |
Количественное содержание, мг/100 г, |
||
|---|---|---|---|
| Полифенолы в расчете на пирогаллол | Флавоноиды в пересчете на гиперозид | Иридоиды, рассчитанные по отношению к ацетату гарпагида | |
| С настойкой пустырника | 167 ± 11 * | 17 ± 4 ** | 57 ± 2*** |
| С лизином | 163 ± 6 | 16 ± 1 | 51 ± 3 |
| С аспарагиновой кислотой | 162 ± 8 | 19 ± 2 | 58 ± 2 |
| С лейцином | 166 ± 7 | 15 ± 4 | 52 ± 1 |
| С аланином | 169 ± 10 | 16 ± 3 | 53 ± 2 |
| С фенилаланином | 174 ± 5 | 14 ± 4 | 55 ± 1 |
| С глицином | 161 ± 13 | 12 ± 3 | 61 ± 3 |
| С валином | 168 ± 5 | 15 ± 4 | 56 ± 2 |
| С гистидином | 158 ± 9 | 16 ± 2 | 57 ± 2 |
| С глутаминовой кислотой | 164 ± 11 | 18 ± 1 | 54 ± 1 |
| С аргинином | 161 ± 8 | 13 ± 2 | 60 ± 2 |
| С цистеином | 169 ± 7 | 15 ± 3 | 59 ± 2 |
| С метионином | 165 ± 4 | 16 ± 4 | 55 ± 1 |
Различия в содержании БАВ в экстрактах с аминокислотами и без них по t -критерию считали недостоверными при * p = 0,64, ** p = 0,27 и *** p = 0,18.
Таблица 3. Характеристики суммарных ультрафиолетовых (УФ) спектров поглощения экстрактов пустырника.
| Извлекать | λ 1 макс. | А 1 | λ 2 макс. | А 2 | А 1 /А 2 |
|---|---|---|---|---|---|
| С настойкой пустырника | 285 | 0,158 | 326 | 0,161 | 0,98 |
| С аргинином | 281 | 0,537 | 324 | 0,517 | 1,04 |
| С валином | 282 | 0,273 | 326 | 0,267 | 1,02 |
| С фенилаланином | 280 | 0,428 | 331 | 0,360 | 1.19 |
| С аланином | 281 | 0,362 | 324 | 0,345 | 1,05 |
| С аспарагиновой кислотой | 292 | 0,211 | 327 | 0,214 | 0,99 |
| С глицином | 288 | 0,509 | 328 | 0,509 | 1,00 |
| С лизином | 288 | 0,582 | 326 | 0,576 | 1.01 |
| С лейцином | 289 | 0,467 | 328 | 0,473 | 0,99 |
| С гистидином | 278 | 0,541 | 327 | 0,542 | 1,00 |
| С цистеином | 285 | 0,458 | 326 | 0,434 | 1,06 |
2.2. Исследование психотропной активности экстрактов
Результаты исследований влияния экстрактов пустырника, модифицированных аминокислотами, на поведенческие реакции лабораторных крыс в условиях открытого поля приведены в Таблица 4 и Рисунок 1.
Рисунок 1. Приведены результаты распределения видов активности экстрактов пустырника на поведенческие реакции лабораторных крыс в тесте «открытое поле».
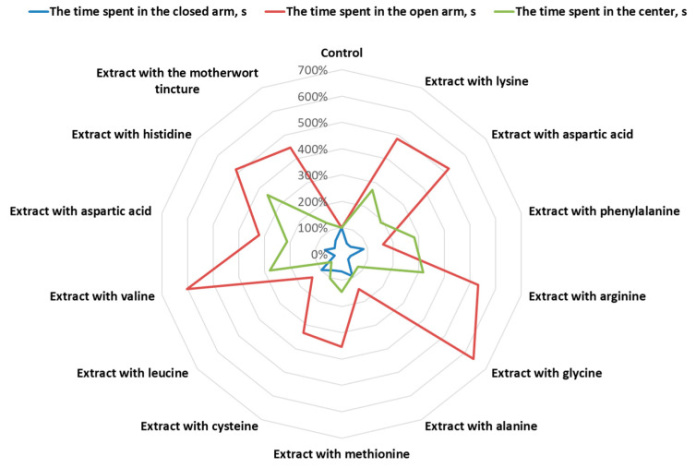
Таблица 4. Приведены результаты изучения влияния экстрактов пустырника на поведенческие реакции лабораторных крыс в тесте «открытое поле».
| Экспериментальная группа животных | Количество зарегистрированных действий | |||||||
|---|---|---|---|---|---|---|---|---|
| Пересечения | Вертикальные позы | Заглянуть в дыры |
Исследовательская деятельность: ∑ позы + отверстия |
Дефекация | Мочеиспускание | Мойка |
Эмоциональная реакция: ∑ болюсы + мочеиспускание + груминг |
|
| Контроль | 28,67 ± 1,75 | 5,67 ± 0,52 | 3,83 ± 0,82 | 4,75 ± 1,14 | 2,50 ± 0,84 | 2,00 ± 0,63 | 1,83 ± 0,75 | 2,11 ± 0,76 |
| Извлекать | ||||||||
| С лизином | 39,17 ± 4,45 * | 8,00 ± 0,63 * ,## | 4,00 ± 0,89 | 6,00 ± 2,22 | 1,17 ± 0,41* ,# | 1,67 ± 0,52 | 1,17 ± 0,41 | 1,33 ± 0,49* ,# |
| С аспарагиновой кислотой | 38,67 ± 14,53 | 8,0 ± 1,79** | 2,83 ± 0,75 | 5,42 ± 3,06 | 1,17 ± 0,41* ,# | 1,50 ± 0,55 | 1,33 ± 0,82 | 1,33 ± 0,59* ,# |
| С лейцином | 17.00 ± 6.20 * ,# | 3,00 ± 1,67* ,# | 2,17 ± 0,75 * | 2,58 ± 1,31* ,# | 1,17 ± 0,41* ,# | 1,17 ± 0,41 ** ,## | 1,33 ± 0,52 | 1,22 ± 0,43* ,# |
| С аланином | 18,17 ± 1,17 * ,# | 4,17 ± 0,75 * ,## | 1,67 ± 0,52 * ,## | 2,92 ± 1,44 * ,## | 3,83 ± 1,17 ** ,## | 1,17 ± 0,41 ** ,## | 0,83 ± 0,41 ** ,## | 1,94 ± 1,55 |
| С фенилаланином | 33,33 ± 4,97 | 7,83 ± 4,88 | 6,33 ± 0,82* ,# | 7,08 ± 3,42** | 2,50 ± 0,84 | 1,33 ± 0,52 | 1,50 ± 0,84 | 1,78 ± 0,88 |
| Контроль | 21,67 ± 1,21 | 4,67 ± 0,82 | 2,83 ± 0,75 | 3,75 ± 1,22 | 2,33 ± 0,82 | 2,00 ± 0,63 | 1,67 ± 0,82 | 2,00 ± 0,77 |
| Извлекать | ||||||||
| С глицином | 62,50 ± 1,87* ,# | 7,83 ± 1,17 * | 5,17 ± 1,17 * ,## | 6,50 ± 1,78 * ,## | 1,33 ± 0,52 ** ,# | 1,00 ± 0,00 ** ,## | 1,17 ± 0,41 | 1,17 ± 0,38 * ,# |
| С валином | 71,33 ± 4,80* ,# | 7,17 ± 1,17 * | 5,00 ± 0,63 * ,## | 6,08 ± 1,44 * | 1,50 ± 0,55 # | 0,83 ± 0,41* ,# | 1,17 ± 0,41 | 1,17 ± 0,51* ,# |
| С гистидином | 48,50 ± 2,74* ,# | 6,33 ± 1,03** | 2,50 ± 0,55 | 4,42 ± 2,15 | 1,67 ± 0,52 # | 1,33 ± 0,52 | 1,33 ± 0,52 | 1,44 ± 0,51** ,# |
| С глутаминовой кислотой | 46,67 ± 2,16* ,# | 5,50 ± 1,05 | 1,50 ± 0,55 * | 3,50 ± 2,24 | 1,00 ± 0,00** ,# | 1,00 ± 0,00 * ,# | 1,33 ± 0,52 | 1,11 ± 0,32 * ,# |
| Контроль | 23,50 ± 1,87 | 4,50 ± 0,84 | 2,50 ± 1,05 | 3,50 ± 1,38 | 2,83 ± 0,75 | 2,17 ± 0,75 | 2,17 ± 0,75 | 2,39 ± 0,78 |
| Извлекать | ||||||||
| С аргинином | 42,50 ± 2,88 * | 6,67 ± 1,21 * | 5,83 ± 1,47* ,# | 6,25 ± 1,36 * ,## | 2,33 ± 1,03 | 1,17 ± 0,41 ** ,## | 1,67 ± 0,82 | 1,72 ± 0,89** |
| С цистеином | 39,00 ± 7,95 * | 6,33 ± 1,03 * | 4,00 ± 1,10** | 5,17 ± 1,59** | 1,67 ± 0,52 ** ,## | 1,50 ± 0,55 | 1,33 ± 0,52 | 1,50 ± 0,51 * ,# |
| С метионином | 29,67 ± 3,01* ,# | 6,83 ± 0,75 * | 4,17 ± 1,17** | 5,50 ± 1,68 * | 3,00 ± 0,89 | 1,33 ± 0,52 | 1,17 ± 0,41** | 1,83 ± 1,04 |
| С настойкой пустырника (референс) | 39,67 ± 1,63 * | 6,17 ± 1,47** | 2,17 ± 0,75 | 4,75 ± 1,96 | 2,33 ± 0,52 | 2,00 ± 0,63 | 1,83 ± 0,75 | 2,06 ± 0,64 |
* — достоверно по сравнению с контрольной группой при р < 0,01;
** — достоверно по сравнению с контрольной группой при р < 0,05;
# — достоверно по сравнению с группой препаратов сравнения при p < 0,01;
## — достоверно по сравнению с группой препаратов сравнения при p < 0,05.
Дозы аминокислот в полученных экстрактах были значительно ниже описанных в литературе и обеспечивали определенный фармакологический эффект. В связи с этим изучать их как отдельные вещества было нецелесообразно.
Результаты исследований модифицированных сухих экстрактов пустырника в тестах приподнятого крестообразного лабиринта приведены в Таблица 5 и фигура 2.
фигура 2. Результаты распределения видов активности экстрактов пустырника в тесте приподнятого крестообразного лабиринта.
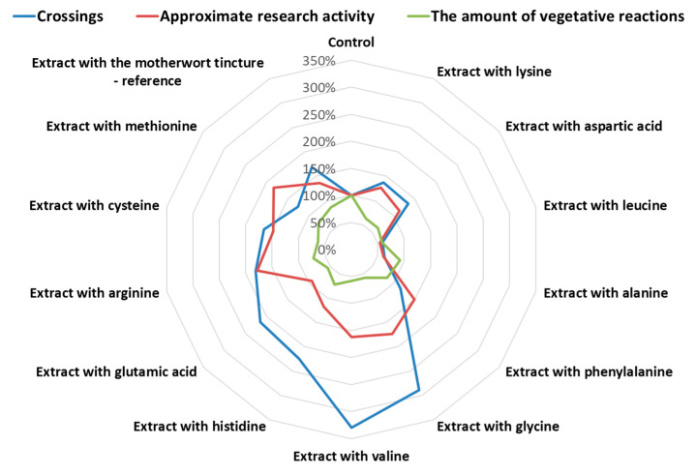
Таблица 5. Результаты исследования модифицированных сухих экстрактов пустырника в тесте приподнятого крестообразного лабиринта.
| Экспериментальная группа животных | Время нахождения в закрытом рукаве, с | Время нахождения в открытом рукаве, с | Количество входов в закрытую руку | Количество входов в Open Arm | Время нахождения в центре, с |
|---|---|---|---|---|---|
| Контроль | 153,7 ± 3,2 | 19,8 ± 1,3 | 5,0 ± 0,6 | 4,8 ± 0,4 | 6,5 ± 3,0 |
| Извлекать | |||||
| С лизином | 66,3 ± 1,4 * ,## | 96,2 ± 4,2* ,# | 4,5 ± 0,5 | 6,3 ± 0,5 # | 17,5 ± 3,1 * |
| С глутаминовой кислотой | 64,5 ± 2,0 * | 103,2 ± 2,5* ,# | 6,8 ± 0,8 * ,## | 4,5 ± 0,9** ,## | 12,3 ± 1,9 * |
| С фенилаланином | 129,7 ± 9,6 * | 32,0 ± 3,9* ,# | 5,0 ± 0,9 | 6,0 ± 0,4** ,# | 18,3 ± 7,8** |
| С аргинином | 53,8 ± 2,5* ,# | 105,5 ± 2,4* ,# | 5,2 ± 0,8 | 5,0 ± 0,0 # | 20,7 ± 3,1 * ,## |
| С глицином | 49,5 ± 4,0 * | 127,0 ± 6,7* ,# | 4,3 ± 1,0 | 7,3 ± 1,0 * ,## | 5,2 ± 2,1 |
| С аланином | 144,5 ± 2,9 * | 29,5 ± 3,2* ,# | 7,3 ± 1,4 * ,## | 6,3 ± 1,4 ** ,## | 6,0 ± 2,4 |
| Контроль | 152,5 ± 3,7 | 19,0 ± 2,1 | 4,5 ± 1,0 | 4,3 ± 0,8 | 8,5 ± 2,7 |
| Извлекать | |||||
| С метионином | 100,5 ± 2,3 * | 67,2 ± 2,9* ,# | 4,8 ± 1,5 | 5,5 ± 1,0 | 12,3 ± 2,4** |
| С метионином | 107,8 ± 5,1 * | 63,3 ± 4,1* ,# | 7,0 ± 1,4 * | 5,3 ± 0,8 | 8,8 ± 3,6 |
| С лейцином | 148,7 ± 2,4 ## | 27,2 ± 1,9* ,# | 6,8 ± 1,6** | 6,2 ± 0,8 * | 4,2 ± 2,2 ** ,## |
| С гистидином | 51,8 ± 2,3* ,# | 97,7 ± 3,6* ,# | 5,7 ± 1,2 | 7,0 ± 1,4 * | 30,5 ± 4,0* ,# |
| С валином | 41,8 ± 3,9* ,# | 114,3 ± 4,7* ,# | 3,3 ± 1,0 # | 5,3 ± 1,0 | 23,8 ± 2,3* ,# |
| С аспарагиновой кислотой | 101,0 ± 2,6 * ,## | 61,0 ± 1,4* ,# | 7,2 ± 0,8 * ,## | 4,8 ± 0,8 ## | 18,0 ± 1,3 * ,## |
| Настойка пустырника | 83,7 ± 7,9 * | 85,3 ± 6,7 * | 5,5 ± 1,0 | 6,2 ± 0,8 * | 11,0 ± 6,2 |
*— р ≤ 0,01 по отношению к показателю в группе контрольных животных;
**— р ≤ 0,05 по отношению к показателю в группе контрольных животных;
# — р ≤ 0,01 по отношению к показателю в группе животных, принимавших настойку пустырника;
## — р ≤ 0,05 по отношению к показателю в группе животных, получавших настойку пустырника.
Проявление двигательной активности в тесте «открытое поле» определяют по количеству квадратов, пройденных подопытным животным. Согласно полученным результатам, введение экстрактов пустырника в комплексах с валином, глицином, гистидином и глутаминовой кислотой привело к достоверному увеличению этого показателя на 229, 188, 124 и 115 % соответственно. Достоверное увеличение числа пересекаемых квадратов по сравнению с контрольными животными ( p< 0,01) наблюдалось в группах крыс, принимавших экстракты пустырника в сочетании с аргинином (на 81%) и цистеином (на 66%), а также настойку пустырника (на 69%). В то же время в группах животных, получавших дозу экстракта пустырника с лейцином и аланином, эта активность снижалась на 41% и 37% по сравнению с контрольной группой. Остальные исследованные экстракты пустырника в сочетании с аминокислотами проявляли незначительную тенденцию к увеличению показателя двигательной активности.
В группах животных, получавших экстракты пустырника в комплексах с лизином (на 41 %), аспарагиновой кислотой (на 41 %), глицином (на 68 %), валином (на 54 %), наблюдалось увеличение числа прямостоячих поз. , аргинин (на 48%), метионин (на 52%) и цистеин (на 41%). Эти изменения были значимы при p < 0,05 и p < 0,01 по сравнению с контролем. Введение экстрактов пустырника в сочетании с фенилаланином и гистидином, а также настойки пустырника приводило к увеличению показателя на 38 % ( р > 0,05), 36 % ( р < 0,05) и 37 % ( р< 0,05) соответственно. Экстракт пустырника в сочетании с глутаминовой кислотой показал незначительное увеличение числа поз, но результат недостоверен при уровне значимости р < 0,05. В группах животных, получавших экстракт пустырника в сочетании с лейцином и аланином, этот показатель был ниже на 47 и 26 % соответственно по сравнению с контролем.
Исследовательская активность, проявляемая по количеству обследованных в полевых условиях лунок, достоверно повышалась у животных, принимавших экстракты пустырника в комплексах с фенилаланином, глицином, валином, аргинином, цистеином и метионином на 65%, 82%, 76%, 133%, на 60% и 67% соответственно по сравнению с контрольной группой и снижалась у животных, получавших экстракт пустырника в сочетании с лейцином, аланином и глутаминовой кислотой, на 43%, 57% и 47% соответственно. Введение экстрактов пустырника в комплексы с аспарагиновой кислотой и гистидином приводило к недостоверному снижению числа обследованных лунок, тогда как настойка пустырника повышала показатель на 33% (р > 0,05 ) .
Экстракты пустырника в сочетании с аргинином, глицином, валином, метионином, фенилаланином и цистеином достоверно повышали количество поисковых ответов по сравнению с контролем. В то же время экстракты пустырника в сочетании с глицином и аргинином оказывали аналогичное влияние на этот показатель по сравнению с группой животных, получавших настойку пустырника, увеличивая количество ответов (при р < 0,05 ) .
Статистически значимое снижение эмоциональной реакции животного, в частности числа актов дефекации, наблюдалось в группах, получавших экстракт пустырника в сочетании с лизином (на 53%), аспарагиновой кислотой (на 53%), лейцином (на 53%). , глицин (на 47%), глутаминовую кислоту (на 57%) и цистеин (на 41%). Остальные исследованные комплексы не оказывали существенного влияния на реакцию животного.
При оценке влияния исследуемых комплексов на количество мочеиспусканий выявлено статистически значимое снижение показателя в группах животных, получавших экстракты пустырника в сочетании с лейцином (на 42%), аланином (на 42%), глицином (на 50%). %), валин (на 58%), глутаминовую кислоту (на 50%) и аргинин (на 46%).
Достоверные изменения числа актов груминга, т. е. уменьшение, наблюдались при введении экстрактов пустырника в сочетании с аланином и метионином на 55 и 46 % соответственно по сравнению с контрольной группой (р < 0,05 ) .
При оценке суммарного вегетативного проявления реакций животных в стрессовых условиях выявлено достоверное снижение показателей ( р < 0,05) в группах животных, получавших экстракты пустырника с лизином (на 37%), аспарагиновой кислотой (на 37%), цистеином (на 37%). 37%) за счет уменьшения числа актов дефекации, экстракты с валином (на 42%) и аргинином (на 38%) за счет уменьшения количества мочеиспусканий, экстракты с лейцином (на 42%) , глицин (на 42%) и глутаминовую кислоту (на 44%) за счет уменьшения количества дефекаций и мочеиспусканий, экстракт с гистидином (на 38%).
Способность препаратов повышать двигательную активность животных может свидетельствовать об их стимулирующем действии на ЦНС. Этот эффект характерен для препаратов с ноотропной, адаптогенной, нормотимической, актопротекторной и другими активностями. В то же время статистически значимых различий других видов поведенческих реакций на фоне этих фармакологических средств выявлено не было.
Некоторые соединения незначительно повышали активность дефекации крыс в тесте «открытое поле». Это может свидетельствовать об активации парасимпатической периферической нервной системы — обычной реакции высших животных на стресс. Однако соединения, содержащие лейцин, глицин и валин, оказывали вегетостабилизирующее действие; следовательно, можно утверждать, что эти соединения обладают стресс-защитным действием.
3. Обсуждение
В целом фитохимический профиль пустырника очень хорошо изучен и описан в ряде обзоров. В надземных частях пустырника разными авторами идентифицированы различные алкалоиды, дитерпеноиды, тритерпеноиды, иридоидные гликозиды, флавоноиды, стеролы, эфирные масла, фенилпропаноиды, фенольные кислоты, гликозиды, дубильные вещества, пептиды и др. Таким образом, найти что-то новое в химическом составе видов было бы довольно сложно. Однако обнаруженные в нашем исследовании метоксиапигенин, эллаговая кислота и катехин ранее в пустырнике не упоминались. Седативное действие пустырника теоретически связано с иридоидами, в то время как алкалоид леонурин не играет важной роли в деятельности центральной нервной системы, но может быть потенциальным соединением при рвоте и тошноте. Кроме того, гипотензивное и успокаивающее действие пустырника может быть обусловлено иридоидами. Взаимосвязь между химическим составом пустырника и его фармакологическими эффектами пока не ясна.
В экстрактах обнаружено 15 основных веществ фенольной природы, из них идентифицировано 8. В этих экстрактах также было 10 гидроксикоричных кислот, три из которых были идентифицированы (хлорогеновая, кофейная и розмариновая кислоты). Доминирующими гидроксикоричными кислотами были хлорогеновая и кофейная кислоты. Среди флавоноидов идентифицированы катехин, гиперозид и рутин. Следует отметить, что экстракты имели значительное содержание эллаговой кислоты.
Максимумы поглощения сухих модифицированных экстрактов крапивы собачьей, во-первых, находились в диапазоне 281–292 нм, во-вторых, в диапазоне 324–331 нм (Таблица 3). Наибольшие визуально заметные изменения в ультрафиолетовых (УФ) спектрах экстрактов были заметны в диапазоне 281–292 нм, что свидетельствует о взаимодействии аминокислот с ароматической группой. Кроме того, при добавлении аминокислот происходили гипо- и гиперхромные сдвиги в максимумах поглощения. Соотношение поглощения в этих пиках варьировало в зависимости от аминокислоты, что указывало на образование разных комплексов.
В клинических испытаниях было подтверждено, что настойка или масляный экстракт пустырника снижает тревожность и стабилизирует эмоциональное состояние благодаря содержанию иридоидов, как и в других противотревожных лекарственных растениях.
Экстракты пустырника с аланином и лейцином оказывали статистически значимое угнетающее действие на двигательную и исследовательскую активность животных. Они уменьшили количество пересекаемых квадратов на 37% и 41% ( p <0,01), а сумма вертикальных поз и исследованных отверстий уменьшилась на 57% и 43% ( p <0,01).
Такое влияние на поведение крыс можно расценивать как анксиолитическое. Этот эффект характерен для ряда нейротропных препаратов: анксиолитиков, транквилизаторов, стресс-протекторов, антидепрессантов, препаратов с нормотимической, нейролептической и другими активностями. Данный эффект фармакологического средства предсказуем из-за наличия в его составе выраженного анксиолитического действия. Ранее было показано, что иридоиды обладают анксиолитической активностью. Аланин является фактором ЦНС, предотвращающим чрезмерное возбуждение нервной ткани и вызывающим торможение возбуждения. Эта аминокислота проявляет свой анксиолитический эффект посредством взаимодействия с участками рецептора глутамата N-метил-D-аспартата (NMDA), сайтом коагониста глицина на рецепторе NMDA и рецепторами γ-аминомасляной кислоты типа А и С, а также путем ингибирования обратного нейронального захвата гамма-аминомасляной кислоты (ГАМК) и усиления ГАМКергической нейротрансмиссии. Вероятно, аланин потенцирует анксиолитический эффект экстракта пустырника.
Результаты этого эксперимента подтверждают потенциальную пользу использования экстрактов пустырника с аланином при лечении психовегетативных расстройств в качестве симпатического тонизирующего средства.
Так, наибольшей активностью обладали экстракты пустырника в комплексах с валином, глицином, аргинином и цистеином; они приводили к повышению двигательной и исследовательской активности подопытных крыс при снижении показателей эмоционального состояния животных.
Животные интактной контрольной группы (ИК) большую часть времени проводили в темных отсеках (руках). Процентное распределение времени (темные лучи против светлых рукавов против центральной области) для животных группы IC было 85,4% против 11,0% против 3,6%. Этот результат в целом соответствует типичной картине поведения грызунов в новом незнакомом пространстве и соответствует литературным данным.
В первую группу вошли три фармакологических средства: экстракты пустырника с фенилаланином, аланином и лейцином. На фоне этих составов не произошло статистически значимого снижения времени нахождения грызунов в темных отсеках, а показатель времени нахождения животных в светлых отсеках не увеличился. Это свидетельствует о том, что эти средства не устраняли тревогу у крыс, возникшую в связи с их пребыванием в новом незнакомом ярко освещенном пространстве.
В группу экстрактов с умеренной противотревожной активностью вошли собственно настойка пустырника, а также экстракты пустырника с метионином и аспарагиновой кислотой. Эти композиции оказывали мягкое анксиолитическое действие, статистически значимо уменьшая время нахождения крыс в темных рукавах и увеличивая время нахождения в светлых. Таким образом, настойка снижала первый показатель на 45,14 % ( р < 0,01 по отношению к показателю ИК), а второй показатель повышал в 3,5 раза ( р < 0,01). В этих условиях смеси экстрактов пустырника с метионином и аспарагиновой кислотой не оказывали более выраженного противотревожного действия, чем настойка.
Противотревожное действие композиций экстрактов пустырника с аргинином, гистидином, глицином и валином оказалось наиболее выраженным в этих условиях (Рисунок 1). Каждый из этих агентов снижал время пребывания животных в темных отсеках на 64,97%, 66,01%, 67,79% и 72,57% соответственно ( p < 0,01 по сравнению с IC). Кроме того, на фоне действия этих фармакологических средств время нахождения в легком плече увеличилось в 4,3, 4,1, 5,4 и 5,0 раза соответственно (р < 0,01 против ИК). Таким образом, анксиолитический эффект этих композиций по временным показателям в темных и светлых руках статистически значимо ( р < 0,01) превышал аналогичный эффект настойки пустырника. Это может свидетельствовать о потенцирующем действии аминокислот (глицин, валин, аргинин, гистидин), входящих в состав этих экстрактов.
По данным литературы, можно оценить способность фармакологических средств сокращать время пребывания грызунов в темных отсеках более чем на 50 %, а также увеличивать время их пребывания в светлых отсеках в 2–4 раза. рассматривается как эффект, присущий истинным анксиолитикам. Таким образом, с учетом полученных результатов экстракты пустырника с аминокислотами (глицин, валин, аргинин, гистидин) можно рассматривать как перспективные препараты с противотревожной активностью.
Полученные результаты свидетельствуют о наличии анксиолитической активности у исследованных экстрактов пустырника в комплексах с аминокислотами. Экстракты с глицином, валином и аргинином оказались более эффективными в снижении тревожности у животных. К преимуществам изученных экстрактов можно отнести отсутствие действия на мышечный тонус и координацию движений.
Среди исследованных экстрактов пустырника в сочетании с аланином и лейцином выраженный анксиолитический эффект. Эти соединения обладали анксиолитической активностью по сравнению с контролем; однако их противотревожная активность была сопоставима с референтным препаратом.
4. Материалы и методы
4.1. Растительный материал
Объектом исследования служила официнальная настойка пустырника (партия 150416, ООО ООО ДКП «Фабрика фармацевтических препаратов Вишфа», Житомирская обл., с. Станишовка Житомирской обл., Украина), из которой получали сухие экстракты.
Для стандартизации настойки пустырника использовали ГФУ 2.0 «Настойка пустырника Н», содержащую такие показатели, как описание свойств, и нормировали следующие идентификационные параметры: содержание этанола (64–69%), сухой остаток (не менее 1,5 %), флавоноиды (не менее 0,01% в пересчете на гиперозид).
4.2. Реагенты
Для модификации настойки пустырника использовали ряд аминокислот: лизин, аспарагиновую и глутаминовую кислоты, лейцин, аланин, фенилаланин, глицин, валин, гистидин, аргинин, цистеин, метионин (набор аминокислот № 2 большой ТУ 6-09-3147-91, Комплект химреактивов).
Для получения экстрактов использовали сахарозу (Compri Sugar O, Witec Industrial, Одесса, Украина) и этанол (Биолик, Мелитополь, Украина).
Для ТСХ, ВЭЖХ и спектрофотометрических исследований использовали следующие реактивы класса «х.ч.» и «х.ч. для анализа»: уксусная кислота ледяная (100063.2500, Merck, Дармштадт, Германия), этилацетат (Химрезерв, Киев, Украина) , хлороформ (102444.1000, Мерк), метанол (106007.2500, Мерк); диметиламинобензальдегид (156477 Sigma-Aldrich, Сент-Луис, Миссури, США), соляная кислота (141020.1214, Merck), гидроксиламин (255580 Sigma-Aldrich, США) и оксид алюминия (010091, Реахим, Харьков, Украина).
Стандартные вещества производства Sigma-Aldrich, США (хлорогеновая кислота С3878, кофейная кислота С0625, гидрат рутина R5143, эллаговая кислота Е2250, кверцетин 3- d -галактозид 83388, розмариновая кислота R4033, (+)-катехина гидрат С1251, 8-ацетилгарпагид SMB00118) использовали для анализа.
4.3. Оборудование
Полученные экстракты получали с использованием сухожарового шкафа ГП-20 (Украина) и вакуумно-циркуляционного аппарата (ЗОИБКД, Чжэнчжоу, Хэнань, Китай).
Исследования фенольных соединений экстрактов проводили методом ВЭЖХ на жидкостном хроматографе Shimadzu LC20 Prominence в модульной системе, оснащенной четырехканальным насосом LC20AD, термостатом колонки STO20A и автоматическим пробоотборником SIL20A.
Количественное содержание основных групп БАВ (сумма полифенолов, флавоноидов и иридоидов) в экстрактах определяли методом абсорбционной спектрофотометрии на спектрофотометре УФ-видимого света Evolution TM 60S (Thermo Fisher Scientific, Waltham, MA, USA).
4.4. Получение экстрактов
Для модификации настойки пустырника и получения модифицированных сухих экстрактов использовали ряд аминокислот: лизин, аспарагиновую и глутаминовую кислоты, лейцин, аланин, фенилаланин, глицин, валин, гистидин, аргинин, цистеин, метионин (комплекс аминокислот № 2 большая ТУ 6-09-3147-91, Комплект химреактивов). Об образовании комплексов можно было заключить из следующих наблюдений: изменились физические свойства экстрактов, они стали лучше растворимы в воде; ТСХ-профиль экстрактов изменился, появились новые пятна, которых раньше не было; общий УФ-спектр экстрактов изменился; когда экстракты анализировали с помощью анализатора аминокислот, можно было видеть, что количество свободной аминокислоты было меньше, чем количество добавленной к экстракту.
Ранее была обоснована технология получения сухой настойки травы пустырника. Он предполагает замену спирта сухим вспомогательным веществом (сахароза, маннит, сорбит и др.). Полученный продукт имеет благоприятные технологические показатели: удовлетворительные объемные свойства, меньшую гигроскопичность, стабильность при хранении. К 50 мл настойки пустырника (44,97 г) добавляли соответствующие аминокислоты в тройном эквимолярном количестве по отношению к количеству фенольных соединений (лизина гидрохлорида (0,273 г), аспарагиновой (0,187 г) и глутаминовой (0,220 г). кислоты, лейцин (0,197 г), аланин (0,133 г), фенилаланин (0,250 г), глицин (0,112 г), валин (0,175 г), гидрохлорид гистидина (0,287 г), аргинин (0,262 г), цистеин (0,182 г) и метионин (0,223 г)). Полученную смесь оставляли настаиваться на сутки для получения комплексов фенольных соединений с аминокислотами, после чего раствор упаривали до 1/20 прежнего объема при температуре 85–95 °С в вакуум-циркуляционном аппарате с вакуумом 680–700 мм рт. ст. и добавляли 20–30 г сахарозы. Смесь сушили и добавляли сахарозу (44,97 г) перед растиранием в ступке до образования однородной массы. Полученные экстракты сушили в сухожаровом шкафу при температуре 50–60 °С до влажности не более 5 %. В качестве препарата сравнения использовали сухой экстракт на основе настойки и сахарозы, полученный аналогичным способом.
4.5. ТСХ анализ экстрактов
Для предварительного анализа и идентификации основных действующих веществ в экстрактах использовали метод ТСХ. Вещества, имеющие фенольную природу, идентифицировали с достоверными образцами флавоноидов и гидроксикоричных кислот с использованием системы растворителей ледяная уксусная кислота Р–вода Р–этилацетат Р (20:20:60). Хроматограмму проявляли с использованием раствора диметиламинобензальдегида; затем пластину прогревали при температуре 100–105 °С в течение 10 мин до появления пятен и исследовали при дневном свете.
Иридоиды идентифицировали методом ТСХ с надежными образцами в системе растворителей хлороформ–метанол–вода (80:2:0,1) по возрастанию. Хроматограмму проявляли с использованием реактива Шталя (1,0 г п -диметиламинобензальдегида в смеси с 50,0 мл уксусной кислоты, 5,0 мл фосфорной кислоты и 100,0 мл воды).
4.6. Подготовка проб, ВЭЖХ-анализ с диодной матрицей и количественный анализ
Всего 50,0 мг (точная масса) экстрактов пустырника сердечного взвешивали в мерной пробирке объемом 5,0 мл и доводили до метки 90% водным метанолом. После 30 мин пребывания в ультразвуковой ванне образец оставляли при комнатной температуре на 3–4 ч. Затем пробирку снова помещали в ультразвуковую ванну на 15 мин, предварительно профильтровав раствор через тефлоновый фильтр с размером пор 0,45 мкм во флакон для анализа.
Исследования фенольных соединений пустырника сердечного.экстракты проводили методом ВЭЖХ на жидкостном хроматографе Shimadzu LC20 Prominence в модульной системе, оснащенной четырехканальным насосом LC20AD, термостатом колонки STO20A и автоматическим пробоотборником SIL20A в следующих условиях: размер – 250 мм × 4,6 мм, размер частиц – 5 мм. мкм; температура колонки - 35°С; длина волны детектирования — 330 нм (гидроксикортиковые кислоты, гликозиды флавоноидов), 370 нм (флавоноидные агликоны), 280 нм (танины), 340 нм (кумарины); скорость потока подвижной фазы — 1 мл/мин; объем вводимой пробы — 5 мкл; подвижная фаза – элюент А, 0,1% раствор трифторуксусной кислоты в воде и элюент Б, 0,1% раствор трифторуксусной кислоты в ацетонитриле. Соотношение элюентов А и Б изменялось в зависимости от времени элюирования: 0–5 мин — 95 к 5, 5–35 мин — 95 → 75 к 5 → 25, 35–40 мин 75 к 25, 40–60 мин 75 → от 50 до 25 → 50, 60–65 мин — 50 → 20–50 → 80, 65–70 мин — 20–80 и 70–85 мин — 95–5 соответственно. Идентификацию фенольных соединений проводили в зависимости от времени удерживания стандартов и УФ-спектральных характеристик.
4.7. Количественное содержание основных групп БАВ методом абсорбционной спектрофотометрии.
Количественное содержание основных групп БАВ (сумма полифенолов, флавоноидов и иридоидов) в экстрактах пустырника сердечного определяли методом абсорбционной спектрофотометрии на спектрофотометре УФ-видимого света Evolution TM 60S (Thermo Fisher Scientific, США).
4.8. Определение количественного содержания общих полифенолов
Количественное определение количества полифенолов в расчете на пирогаллол проводили по методике Государственной фармакопеи Украины (ГФУ) 2.0.
4.9. Определение количественного содержания общих флавоноидов
Содержание флавоноидов в экстрактах пустырника определяли спектрофотометрическим методом в расчете на гиперозид по ГФУ с использованием исходных, опытных и компенсационных растворов. Оптическую плотность исследуемого раствора измеряли через 30 мин по отношению к компенсационному раствору при длине волны 425 нм. Содержание суммы флавоноидов в пересчете на гиперозид (%) рассчитывали по следующей формуле:
(А × 0,625)/м,
где А — оптическая плотность исследуемого раствора при 425 нм, m — масса сухого экстракта пустырника, г. Использовали удельную абсорбцию гиперозида, равную 500.
4.10. Определение количественного содержания иридоидов.
Содержание иридоидов в экстрактах пустырника определяли спектрофотометрическим методом в расчете на ацетат гарпагида.
Приблизительно 5 г сухого экстракта (точная масса) помещали в круглодонную колбу вместимостью 100 мл, разбавляли 50 мл 40%-ного этилового спирта и нагревали на кипящей водяной бане с обратным холодильником в течение 45 мин. Экстракт охлаждали и фильтровали через ватный тампон в мерную колбу вместимостью 100 мл. Раствор разбавляли до нужного объема 40% этиловым спиртом (Раствор А). Затем 10 мл раствора А упаривали до 5 мл. Полученный раствор количественно переносили в мерную колбу вместимостью 10 мл и доводили до объема водой. Затем его фильтровали через стеклянную колонку диаметром 1 см с 3 г оксида алюминия II степени активности.
Далее 5 мл элюата помещали в мерную колбу вместимостью 25 мл, добавляли 5 мл щелочного раствора гидроксиламина и выдерживали 5 мин. Затем добавляли 10 мл 1 М раствора соляной кислоты, предварительно разбавляя до объема 1% раствором хлорида железа (III) в 0,1 М растворе соляной кислоты и перемешивая.
Оптическую плотность полученного раствора измеряли на спектрофотометре при длине волны 512 нм. В качестве раствора сравнения использовали смесь, приготовленную в мерной колбе вместимостью 25 мл, при этом 10 мл 1 М раствора соляной кислоты добавляли к 5 мл раствора гидроксиламина перед доведением до объема 1% раствором хлорида железа (III). в 0,1 М растворе соляной кислоты.
Количество иридоидов в экстракте по отношению к ацетату гарпагида (Х) рассчитывали по следующей формуле:
X = (A × 25 × 100 × 100 × 100)/(56 × m × 5 × (100 − w)),
где А — оптическая плотность исследуемого раствора, 56 — удельная абсорбция эталона ацетата гарпагида, m — масса экстракта, г, w — влажность экстракта, %.
4.11. Изучение психотропной активности
Влияние экстрактов пустырника на поведенческие реакции лабораторных белых крыс (массой 200–220 г) изучали в тесте «открытое поле» и в тесте «приподнятый крестообразный лабиринт» [48] на базе ЦНИЛ Национального университета им. Аптека в стандартных условиях на обычном питании при свободном доступе к воде и пище. Животные были разделены на 14 групп по 6 крыс в каждой, из них 12 экспериментальных, одна контрольная и одна контрольная.
Для получения модифицированных экстрактов аминокислоты добавляли в очень малых количествах в следующих терапевтических дозах: лизина гидрохлорид - 0,3 мг/кг; аспарагиновая кислота - 0,21 мг/кг; глутаминовая кислота - 0,24 мг/кг; лейцин — 0,22 мг/кг; аланин — 0,15 мг/кг; фенилаланин — 0,28 мг/кг; глицин — 0,12 мг/кг; валин - 0,19 мг/кг; гидрохлорид гистидина - 0,32 мг/кг; аргинин — 0,29 мг/кг; — 0,2 мг/кг; метионин - 0,25 мг/кг. В таких малых дозах аминокислоты экстрактов не обладают фармакологической активностью; таким образом, нет смысла проверять их по отдельности, так как результаты фармакологического исследования будут такими же, как и у интактных животных.
Исследуемые экстракты вводили перорально в виде водных растворов в дозе 50 мг/кг, соответствующей терапевтической дозе настойки пустырника, за 60 мин до начала опыта. Контрольным животным давали соответствующее количество физиологического раствора.
Измерение показателей поведения крыс определяли в открытом поле размером 100 × 100 см, разделенном на 25 квадратов и 16 отверстий («нор»). В тесте «открытое поле» регистрировали следующие параметры: количество вставаний на задние лапы — вертикальная составляющая ориентировочной реакции, количество перечеркнутых квадратов — горизонтальная составляющая, количество заглядываний в норки — поведение норки, отражающее исследовательская активность, количество актов дефекации, мочеиспускания и груминга — показатель эмоционального состояния животного. Во время теста поиск инициировался путем выхода в центр поля и увеличения количества исследуемых лунок. Время тестирования в тесте «открытое поле» составило 3 мин.
Метод приподнятого крестообразного лабиринта основан на боязни открытого пространства и высоты. Крысу подкладывали мордой к открытому рукаву, после чего регистрировали время нахождения в закрытом и открытом рукавах, количество заходов в закрытый и открытый рукав, продолжительность пребывания в центре. Показатели тревожности включали количество входов в открытые рукава лабиринта, продолжительность пребывания в открытых ответвлениях лабиринта, соотношение времени пребывания в открытых и закрытых ответвлениях, количество пересечений центральной площадки и мочеиспускание, дефекация и уход за телом.
Поскольку в фармакологическом исследовании участвовало несколько лабораторных животных, исследования проводились последовательно. Для каждого блока исследований была своя контрольная группа, для которой проводились расчеты.
4.12. Статистический анализ
Статистическую обработку результатов проводили с использованием t -критерия Стьюдента. Статистические свойства случайных величин с n -мерным нормальным распределением задавались их корреляционными матрицами, которые можно было вычислить из исходных матриц. Материал фармакологического исследования обрабатывали методами вариационной статистики с расчетом средней арифметической и ее стандартной ошибки; достоверность сравниваемых значений оценивали по критериям Стьюдента, Уилкоксона и Манна–Уитни с уровнем вероятности ≤0,05 на компьютере с использованием программ Statistica 6.0, Word и Excel.
5. Выводы
Можно сделать вывод, что в результате фитохимического и фармакологического изучения сухих экстрактов пустырника сердечногол.) настойки, которые были модифицированы 12 аминокислотами, наиболее эффективными веществами с анксиолитической активностью оказались экстракты, модифицированные добавками лизина, глицина, аланина, валина, фенилаланина и аргинина. Эти экстракты могут стать основой для создания новых потенциальных стандартизованных лекарственных средств с психотропной и анксиолитической активностью. Основными оксикоричными кислотами были хлорогеновая и кофейная кислоты, экстракты имели значительное содержание эллаговой кислоты. Среди флавоноидов идентифицированы катехин, гиперозид и рутин. Состав фенольных соединений существенно не различался, а основные отличия касались аминокислот, что, очевидно, сказывалось на общем фармакологическом эффекте.








